.png)

新冠疫苗的进展为各界高度关注,12月23日,国家药审中心受理品种信息显示,国药中生北京生物制品研究所的新冠疫苗上市申请获受理,但蹊跷的是,今日这条信息被撤掉了,不知是否有变故。
同时,路透社报道,智飞生物新冠疫苗在早期和中期试验中被发现是安全的,并能引发免疫反应。该候选药物在早期和中期测试中没有造成严重的不良事件,其常见的轻微副作用仅包括注射疼痛、红肿,而在接受三次不同群体注射的参与者中,至少93%的人检测出了针对新冠病毒的中和抗体。近日,智飞生物新冠疫苗一、二期临床结果预印本上线。
临近年底,创新药的上市申请进展积极。12月22日,东阳光的1类新药磷酸依米他韦胶囊获批上市,成为“人民金融·创新药指数”成分样本中第八个获批上市的品种。近日,和黄医药的索凡替尼胶囊在国内的注册申请进入“在审批”阶段,有望于近期获得批准。
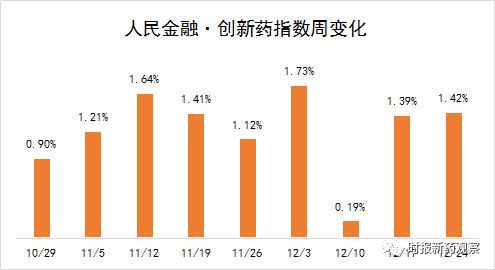
在12月18日至12月24日的发布周期内,来自恒瑞医药、贵州百灵、塔吉瑞等的10个创新药获批临床,我们将其纳入了“人民金融·创新药指数”。截至12月24日,“人民金融·创新药指数”报1303.4点,在最近一个发布周期内上涨了1.42%。目前,“人民金融·创新药指数”的成分样本共有693个。
国药中生新冠疫苗上市申请挂网后又撤下
12月23日,药审中心网站显示,国药中生北京生物制品研究所的新冠病毒灭活疫苗(Vero)上市申请获受理,受理号为CXSS2000061。我国的新冠疫苗一直在药品特殊审批程序通道中,这是新冠疫苗的受理信息首次出现在药审中心网站。
不过,12月24日药审中心网站撤下了该受理信息,截至发稿该受理信息仍未显示。对于受理信息撤下的原因,有可能是需要补充材料,待材料齐备后再次申请上市,或改变申请内容。这类情形在当年9价HPV疫苗审批中出现过,起初默沙东申请9价HPV疫苗临床试验,很快撤销了,改为上市申请并经过一周左右时间获批。还有种情形,或是上市申请重新回到特殊审批通道。
本月初,国药中生的新冠疫苗在阿联酋获批上市。据报道,国药中生提交的III期临床试验中期分析的数据显示,该疫苗预防新冠感染的有效率为86%,中和抗体转阳率为99%,预防中、重度新冠病例的有效率为100%,没有发现严重的安全隐患。
中国科学界内,对新冠疫苗的临床试验数据一直都满怀期待。科兴生物原计划于12月初披露其新冠疫苗三期临床分析数据,12月23日披露时间再次推迟,根据当天公布的初步数据,该疫苗有效性超过50%。
近日,智飞生物重组蛋白新冠疫苗一、二期临床结果通过文献预印形式披露。文章显示,一期临床中,25μg组和50μg组的中和抗体几何平均滴度(GMT)分别为94.5和117.8,二期临床中的25μg组和50μg组的GMT分别为102.5和69.1,超过了COVID-19恢复期样本的水平(GMT,51)。一二期的临床实验数据支持,ZF2001使用25μg疫苗剂量和三针法进行三期临床的安全性和有效性评估。路透社的报道说,智飞生物的新冠疫苗三期临床试验选择低剂量、三针法。
在12月18日至12月24日的发布周期内,除了国药中生的新冠疫苗外,凤凰制药的1.1类中药芪黄胶囊上市申请获受理也获国家药品监督管理局受理;东阳光的1 类新药磷酸依米他韦胶囊获批上市,与索磷布韦联用,治疗成人基因1型非肝硬化慢性丙型肝炎。另外,12月20日,和黄医药的索凡替尼胶囊在国内的注册申请进入“在审批”阶段,有望于近期获得批准,用于治疗晚期非胰腺神经内分泌瘤。
塔吉瑞国际领先创新药获批临床
新发布周期内,来自恒瑞医药、塔吉瑞、贵州百灵等的10个创新药获批临床,我们将其纳入了“人民金融·创新药指数”。目前,“人民金融·创新药指数”的成分样本共有693个。
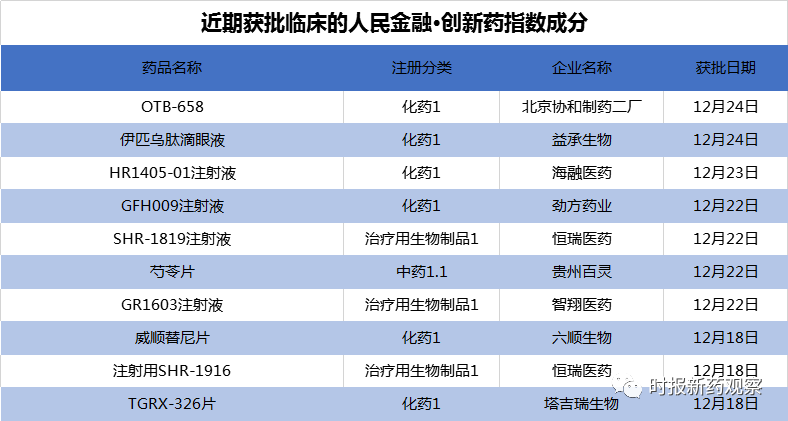
近日,恒瑞医药有两个创新药获得临床批件,分别是SHR-1819和SHR-1916,对应的适应症分别是哮喘和晚期恶性肿瘤。不过恒瑞医药尚未公布这两个创新药的靶点。在恒瑞医药获批临床的创新药中,包括SHR-1916在内,有18个是抗肿瘤药物,占比近半;SHR-1819是恒瑞医药第二个治疗哮喘的创新药,其人源化抗IL-5单克隆抗体SHR-1703注射液正在开展治疗支气管哮喘的1期临床。
塔吉瑞是一家拥有国际领先技术的新药研发企业,已申报包括中国、美国、欧洲、日本等在内的180余项专利。公司创始人王义汉博士在靶向新药领域具有二十余年的研发经验,是已在美国上市的二代ALK抑制剂布格替尼(Alunbrig)的核心发明人。
近日,塔吉瑞自主研发的最新一代ALK/ROS1双重抑制剂TGRX-326获批临床,用于治疗ALK阳性和ROS1阳性晚期非小细胞肺癌。临床前研究显示,TGRX-326新型、独特的药物结构使其对野生型及大多数突变型ALK激酶具有优异的活性和高选择性,具备同类最佳潜质(best-in-class),处于国际领先水平。这是塔吉瑞第二款获批临床的创新药。
此前,塔吉瑞自主研发的第四代Bcr-Abl抑制剂TGRX-678已获得CDE的临床试验批件(受理号:CXHL2000158,CXHL2000159),其作用机制完全不同于现已上市的所有 Bcr-Abl 抑制剂,可用于治疗既往对第一、二、三代抑制剂耐药或不耐受的慢性粒细胞白血病。公司表示,TGRX-326与TGRX-678将一同在2021年初开展首次人体试验。
在临床进展方面,人民金融·创新药数据库监测显示,近日荣昌生物登记启动了RC28-E注射液治疗糖尿病性黄斑水肿的2期临床试验,该药为VEGFR和FGFR双靶标融合蛋白,迪哲医药的DZD1516片、华海药业的HOT-1030注射液、苏州沪云新药的注射用HY0721等登记启动了1期临床。
声明:证券时报力求信息真实、准确,文章提及内容仅供参考,不构成实质性投资建议,据此操作风险自担。

.gif) 证券时报APP
证券时报APP
.gif) 微信公众号
微信公众号